





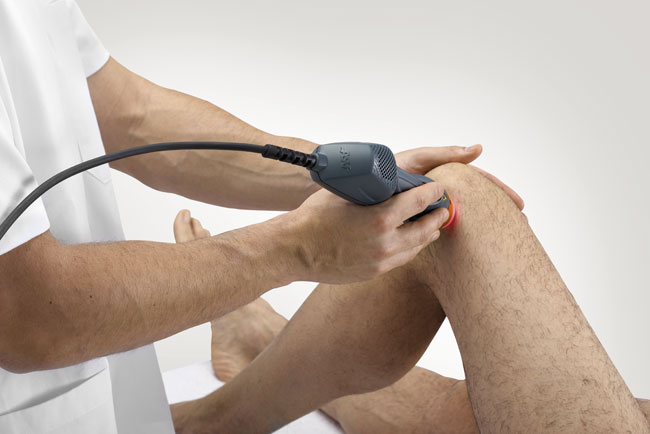
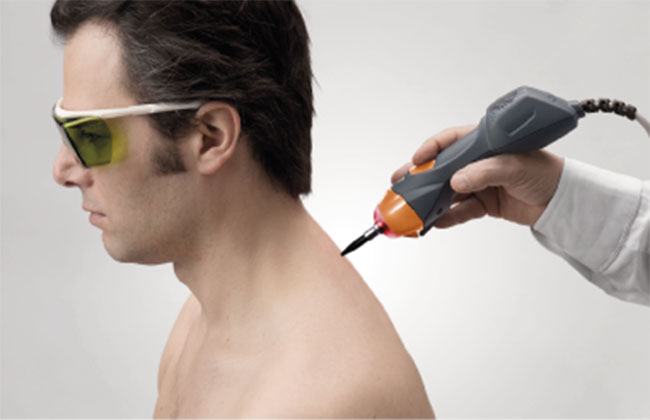
Now is the moment for new ASAlaser devices: the release of Mphi 75, which offers all the features of the Mphi model with the addition of a new handpiece with a peak laser source of 75 Watt, completes the MLS® range by supplying highly specialised treatments such as the cone light guide and pertinent software for laser puncture sessions. The technology, coded by a new software which enables the creation, management and filing of customised protocols for ease of use, is also in the name of innovation. The validity of the new portable device, whose size and weight are appropriate, as a professional partner is ensured by the value acknowledged to MLS® Laser Therapy, whose strong points are recognised as the efficacious anti-inflammatory action, rapid analgesic effect, marked photomechanical effect and the recovery of the peripheral microcirculation. <<Thanks to the new Mphi 75 system – explains Roberto Marchesini, ASAlaser Managing Director – the recognised therapeutic effects and application possibilities of the MLS® family are completed, thereby providing sector professionals with an additional therapeutic solution to rely on for treating, among others, arthrosis, joint and craniofacial pain, haematomas and lumbago issues>>. The inclusion of a new product within the range of the MLS® Laser Therapy devices is part of the 2017/18 development programmes of ASAlaser, a company which has always been at the forefront in implementing state-of-the-art systems and technology focusing on offering a fast rehabilitation and full motor recovery to patients suffering from painful pathologies of the musculo-skeletal apparatus.








L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.