





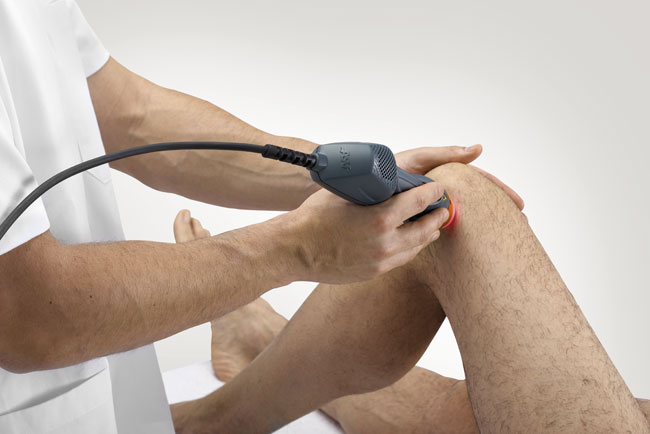
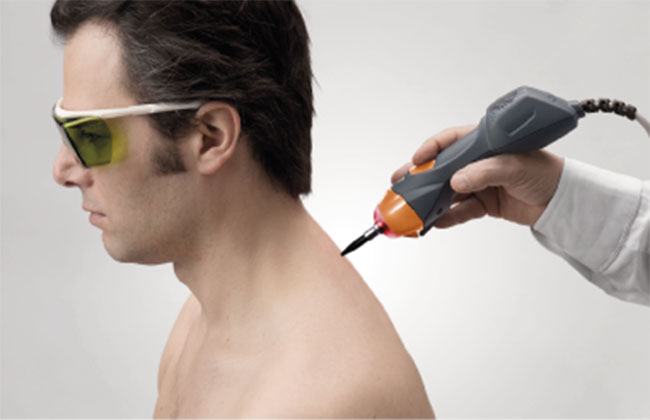
Tiempo de nuevos dispositivos en ASAlaser. Nace Mphi 75 que ofrece todas las funcionalidades del modelo Mphi añadiendo una nueva pieza de mano con fuente láser de 75 Watt de pico, lo que, además de completar la línea MLS®, permite ofrecer unas prestaciones altamente especializadas como la guía de luz cónica y el correspondiente software para aplicaciones de láserpuntura. En la línea de la innovación se encuentra también la tecnología, codificada por un nuevo software que permite crear, gestionar y archivar protocolos personalizados facilitando su uso. Un válido socio profesional del nuevo aparato, portátil y con unas dimensiones y un peso adecuados, es el reconocido valor de la Laserterapia MLS®, que convierte la eficaz acción antiinflamatoria, el rápido efecto analgésico, el marcado efecto fotomecánico y el restablecimiento de las funcionalidades del microcírculo periférico en sus puntos fuertes.<<Gracias al nuevo sistema Mphi 75 – explica Roberto Marchesini, director ejecutivo de ASAlaser – los reconocidos efectos terapéuticos y las posibilidades aplicativas de la familia MLS® se completan al máximo, lo que nos permite poner a disposición de los profesionales del sector una ulterior solución terapéutica con la que poder contar para el tratamiento, entre otras patologías, de la artrosis, los dolores articulares y cráneofaciales, los hematomas y las lumbalgias>>. La introducción de un nuevo producto en la gama de dispositivos para Laserterapia MLS® forma parte de los programas de desarrollo 2017/18 de ASAlaser, que desde siempre está en primera fila en la aplicación de sistemas y tecnologías evolucionados, dirigidos a ofrecer a los pacientes que sufren patologías dolorosas del aparato musculoesquelético una rápida rehabilitación y una plena eficiencia motriz.








L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.