





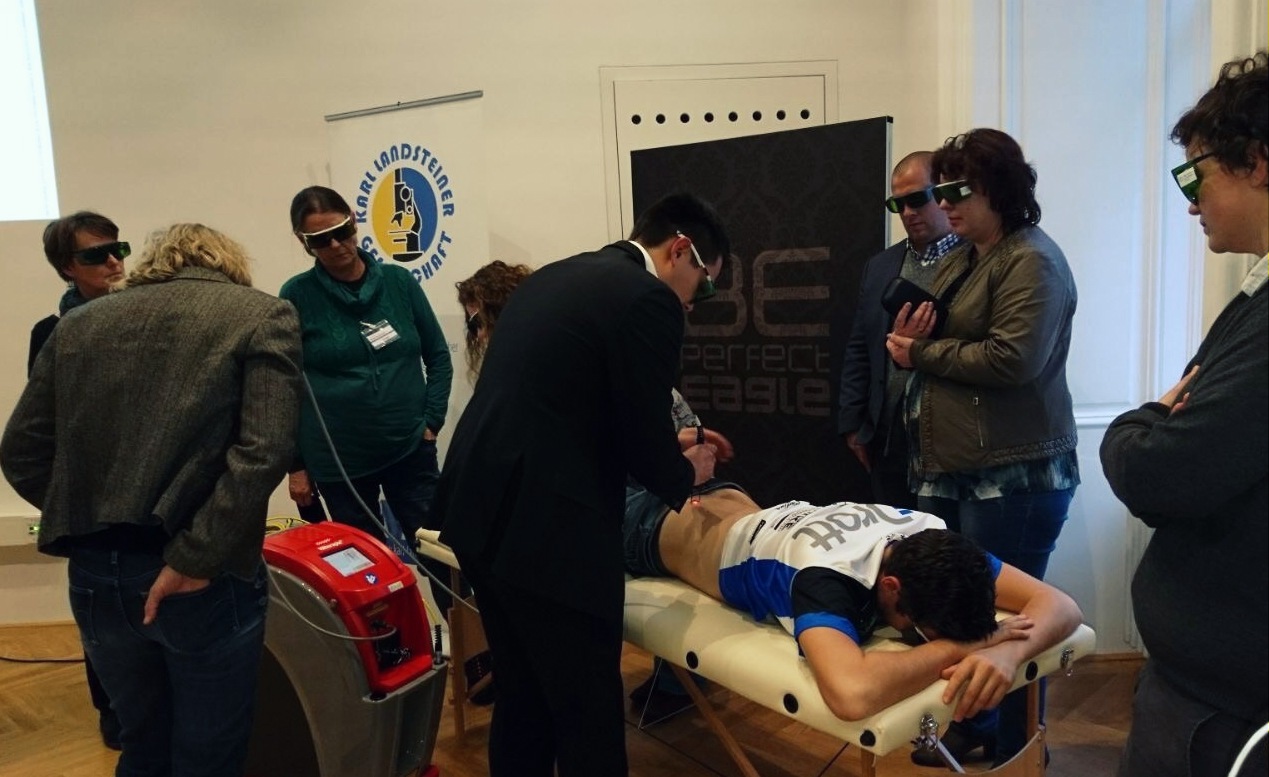
“Lower Back Pain”: this is the theme of the conference "Fachtag Kreuzschmerz" (1 December - Eagle HomeOne, Wien) organised by the head of the Department of Physiotherapy and Rehabilitation of the Wien University Hospital (Dr Michael Quittan). Hilterapia® has carved out a leading role in the program of the meeting through two intervention opportunities: a theoretical one, with a speech held by Dr Tamara Viliani of ASAcampus who analysed in-depth the use and the action of ASA therapy in the treatment of back pain, and a practical-clinical one. In fact, through the direct experience of a physiotherapist who has long been a user of the company's top-performing therapeutic solutions (MLS®, Hilterapia® and Magneto Qs), the participants were able to obtain not only a complete overview of the effects of Hilterapia®, but also to tangibly verify its application on a real patient. The congress participants were also able to examine in depth the use of Hiro 3.0, verifying its simplicity and intuitiveness. "The preparatory activity carried out by Drott, our partner in Austria, together with the support provided in the field by our staff - specifies Roberto Terruzzi, senior ASAlaser Area Manager - have allowed achieving the best results both in terms of understanding the therapy and of the interest and involvement of those present".











L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.