





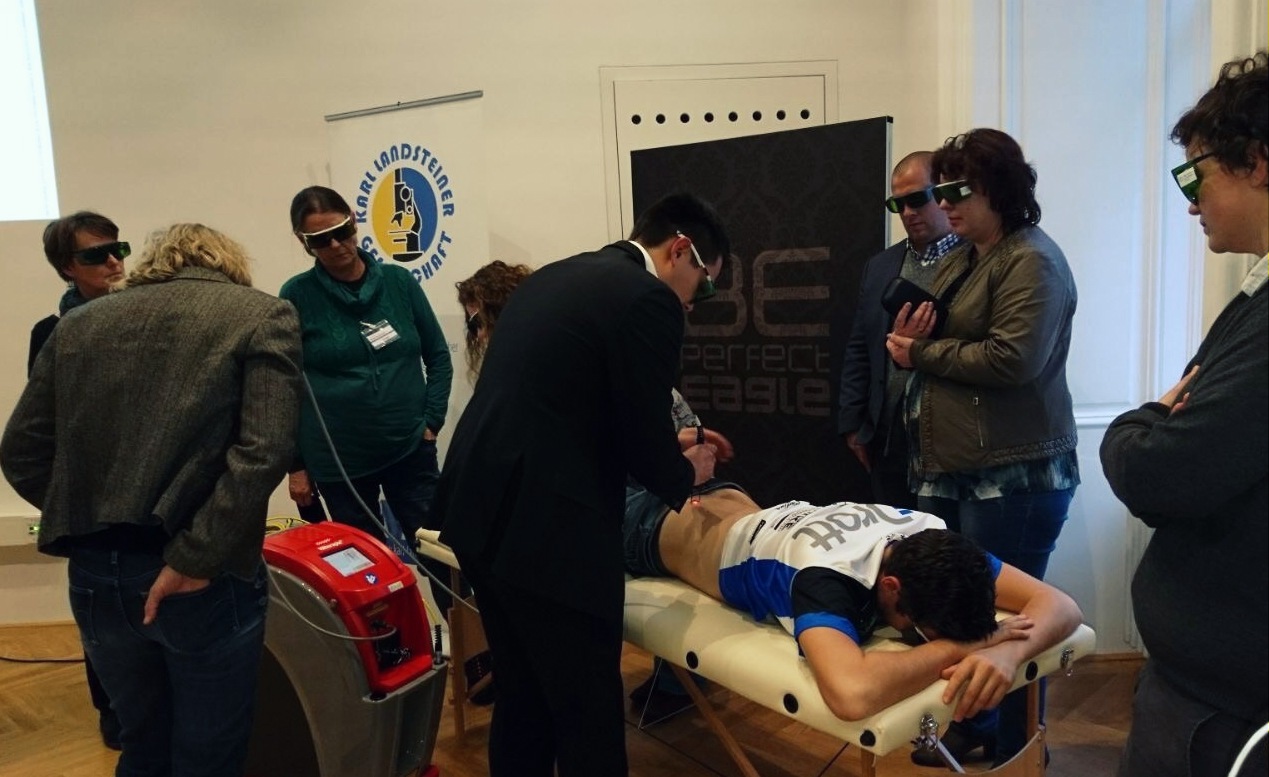
“Lower Back Pain” : questo il tema della conferenza "Fachtag Kreuzschmerz" (1 dicembre - Eagle HomeOne ,Vienna) organizzata dal capo del dipartimento di Fisioterapia e Riabilitazione dell’ospedale universitario di Vienna (Dr. Michael Quittan). Hilterapia® si è ritagliata un ruolo di primo piano nel programma del meeting attraverso due spazi di intervento: uno teorico, affidato ad uno speech della Dr. Tamara Viliani di ASAcampus che ha approfondito l’utilizzo e l’azione della terapia di ASA nel trattamento del mal di schiena, ed uno pratico-clinico. Attraverso infatti l’esperienza diretta di un fisioterapista da tempo utilizzatore delle soluzioni terapeutiche di punta dell’azienda (MLS®, Hilterapia® e Magneto Qs) i partecipanti hanno potuto avere non solo una panoramica degli effetti di Hilterapia®, ma anche verificare in concreto la sua applicazione su un paziente reale. Gli iscritti al congresso hanno infine approfondito anche l’utilizzo del laser Hiro 3.0 constatandone semplicità e intuitività. “L’attività di preparazione svolta da Drott, nostro partner in Austria, unitamente al supporto fornito sul campo dal nostro staff – specifica Roberto Terruzzi, senior Area Manager ASAlaser – hanno permesso il raggiungimento dei migliori risultati sia in termini di comprensione della terapia che di interesse e coinvolgimento dei presenti”.











L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.