





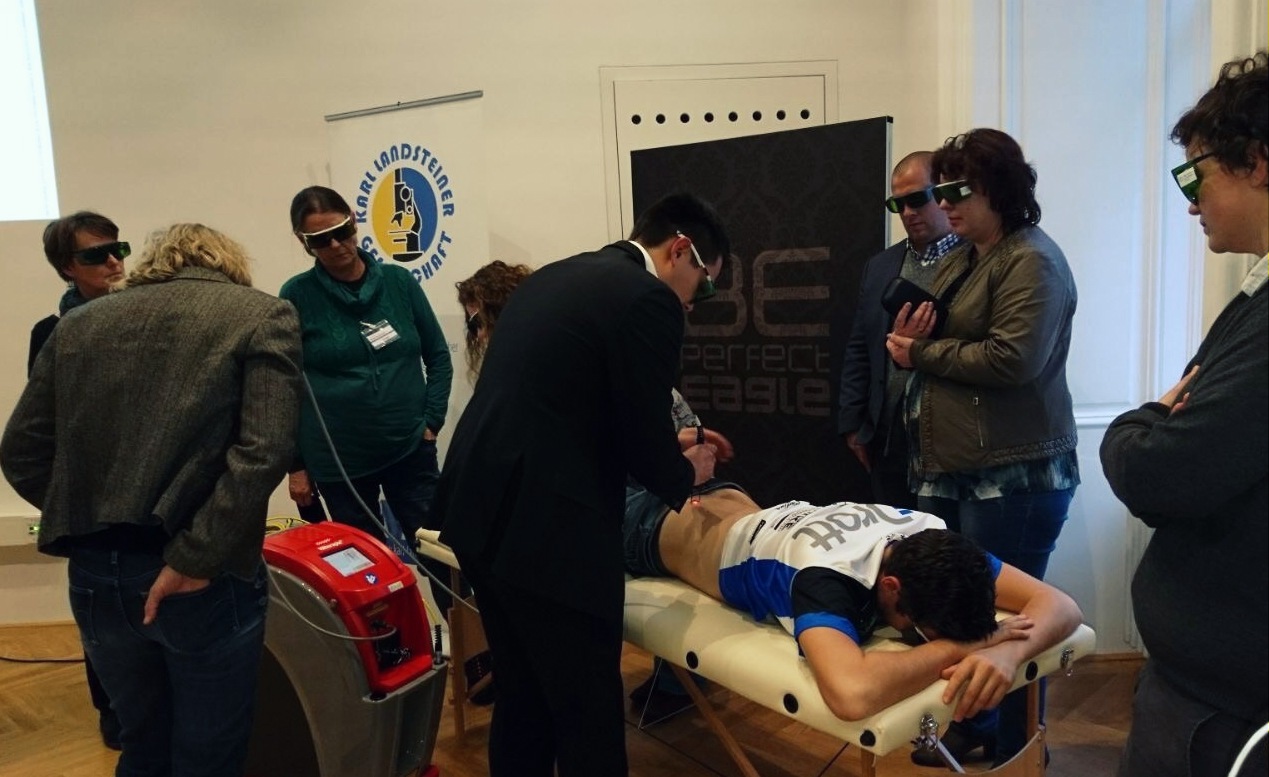
„Lower Back Pain“: Das war das Thema der vom Vorstand des Instituts für physikalische Medizin und Rehabilitation am AKH Wien (Dr. Michael Quittan) organisierten Konferenz „Fachtag Kreuzschmerz“ (1. Dezember, Eagle HomeOne, Wien). Die Hilterapia® nahm dabei eine besonders wichtige Rolle im Programm des Meetings ein, da sie das Thema von zwei Vorträgen war: ein theoretischer Vortrag von Dr. Tamara Vilianivom ASAcampus, in dem die Verwendung und die Wirkung der Therapie von ASA bei der Behandlung von Rückenschmerzen vertieft wurde, und ein praktisch-klinischer Vortrag. Dank der direkten Erfahrung eines Physiotherapeuten, der seit langer Zeit die besten therapeutischen Lösungen des Unternehmens (MLS®, Hilterapia® und Qs Magnetfeldtherapie) anwendet, erhielten die Teilnehmer nicht nur einen Überblick über die Wirkungen der Hilterapia®, sondern konnten auch die Anwendung an einem echten Patienten ausprobieren. Die Kongressteilnehmer haben abschließend auch die Anwendung von Hiro 3.0 getestet und überzeugten sich dabei von der Einfachheit und Intuitivität. „Die Vorbereitungsarbeit von Drott, unserem österreichischen Partner, in Kombination mit der Unterstützung unseres Personals vor Ort“, so Roberto Terruzzi, Senior Area Manager von ASAlaser, „ermöglichten uns die besten Ergebnisse sowohl betreffend das Verständnis der Therapie als auch betreffend das Interesse und die Einbeziehung der Teilnehmer zu erreichen“.











L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.