





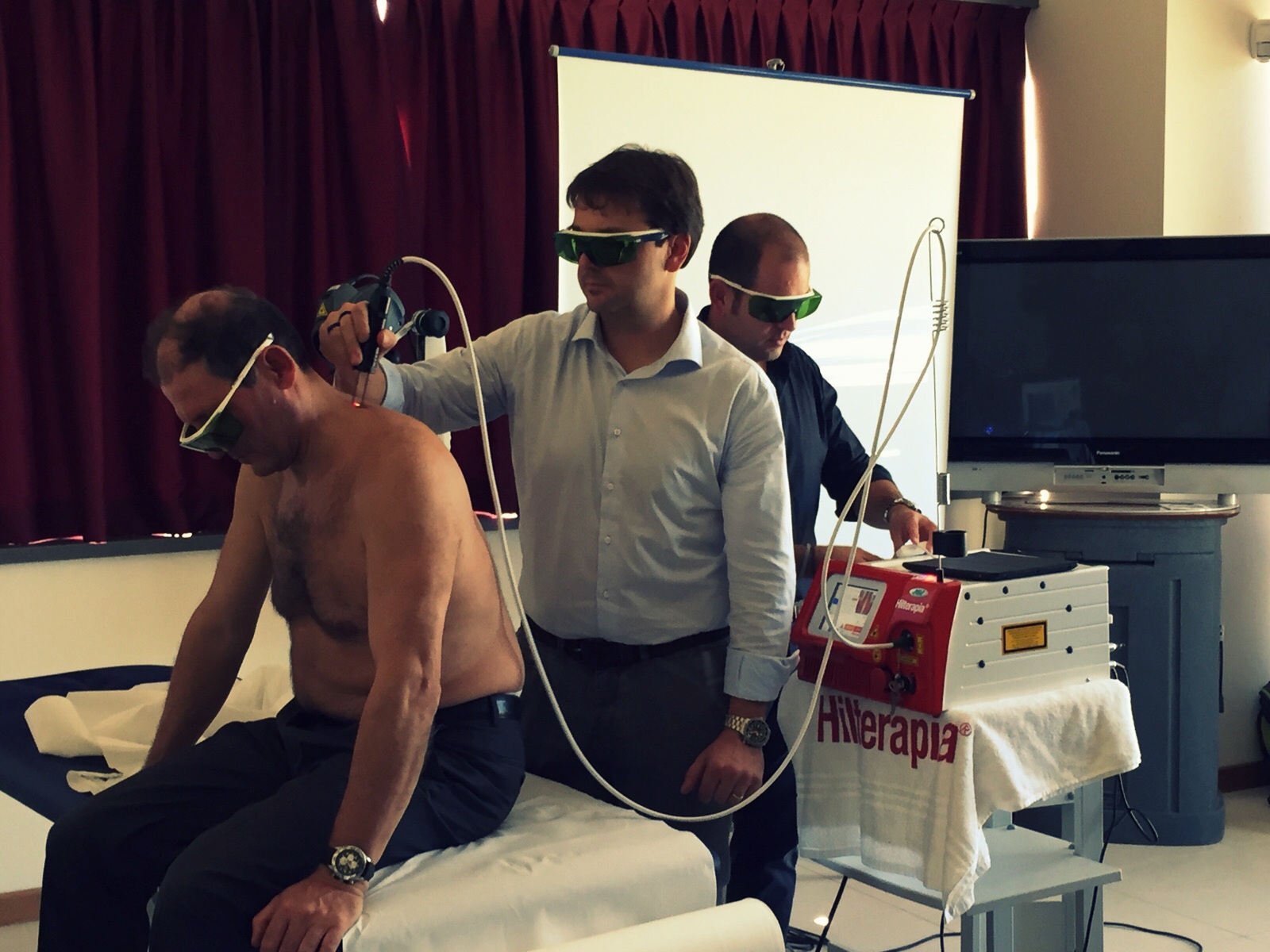
A Faenza nella sede di Medilab-pd, distributore ASAlaser per l'Emilia Romagna, sabato 3 ottobre si è svolto un training teorico e pratico su Laserterapia MLS® e Hilterapia® sotto la guida del Master Trainer Giorgio Dordoni e del Training Coordinator di ASAlaser Alberto Zaghetto. L'argomento della giornata formativa, che ha registrato un'importante affluenza di partecipanti, ha avuto come focus la combinazione delle due metodiche che hanno compiti specifici durante il trattamento. Molto seguita anche la parte pratica, utilissima per dare ulteriore conferma delle potenzialità delle soluzioni terapeutiche ASAlaser e soprattutto per mettere in azione i consigli ricevuti durante il training teorico.
«Questa nuova formula di corso avanzato -ha commentato Giorgio Dordoni- è molto interessante e stimolante perché permette di evidenziare la validità di entrambe le proposte terapeutiche. La possibilità di confrontarsi sia con MLS® che con Hilterapia® ha dimostrato ancora una volta che i risultati sono ottimi se si ha un importante background scientifico alle spalle».
«Ho riscontrato grande interesse da parte dei partecipanti -ha riferito Alberto Zaghetto- che hanno avuto modo di verificare nel concreto l’applicazione delle due terapie così da comprendere quale risulti più idonea per le proprie esigenze e, contemporaneamente, come la loro integrazione possa portare all’eccellenza dei risultati».









L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.