





Background scientifico, campi di applicazione e specifici protocolli di utilizzo in ambito dentale di MLS®: sono questi i punti sviluppati dallo staff ASAlaser nel corso di una sessione training svoltasi a Mannheim (Germania) e rivolta ad alcuni professionisti del settore di riconosciuta fama.
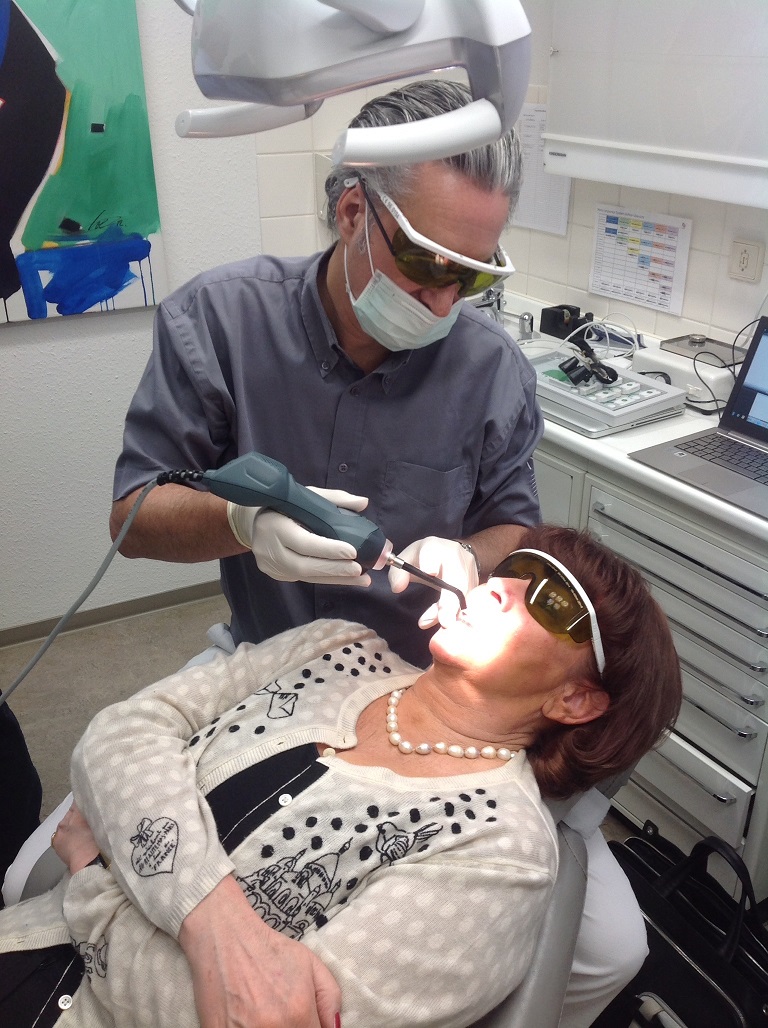
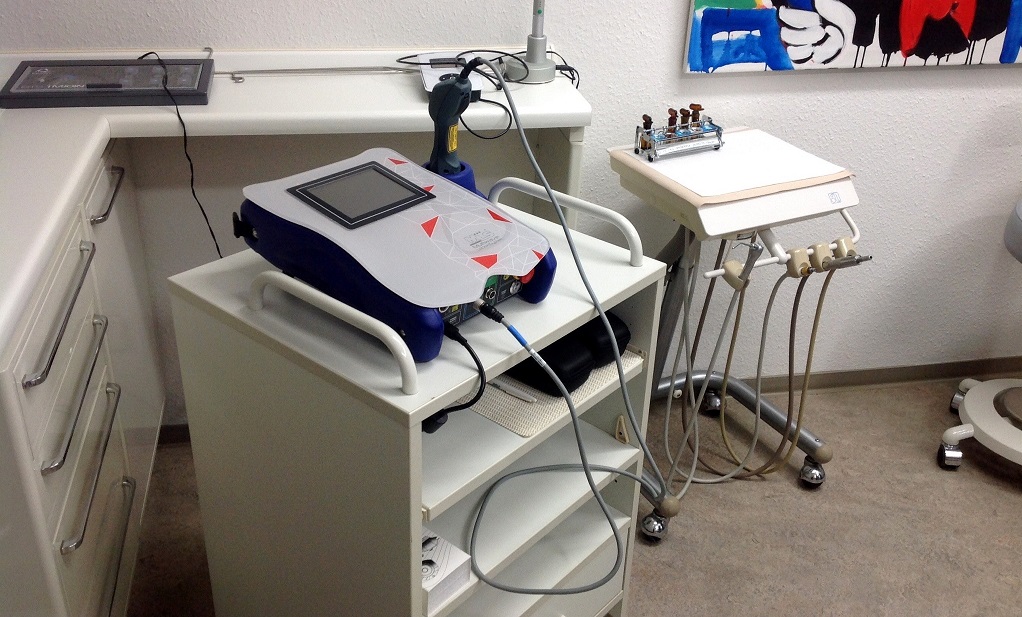
«Il corso – spiega Roberto Terruzzi, Area Manager ASAlaser – è stato articolato in una parte teorica e in una pratica che ha previsto l’impiego del dispositivo Mphi D nel trattare un caso reale. Un paziente affetto da afta linguale è stato infatti sottoposto ad una seduta con MLS® in modo che anche i medici coinvolti potessero verificarne le modalità di applicazione e i risultati ottenibili sin dalle prime applicazioni.» I significativi riscontri ottenuti hanno favorevolmente impressionato i due dentisti esperti in “Neuromuscular Dysbalance” che hanno deciso di dare il via ad uno studio funzionale a comprendere l’efficacia di MLS® nel trattamento dei disordini temporo-mandibolari, del dolore cranio-facciale e dello sbilanciamento neuro-muscolare. «La nostra ambizione – conclude Terruzzi – alla luce dei risultati che saranno ottenuti da questi professionisti, è diffondere nel mercato tedesco la Laserterapia MLS® nel segmento TMD e dolore cranio facciale. Si tratterebbe di un risultato prestigioso per MLS® che, proprio nel comparto dentale, sta raccogliendo riscontri internazionali degni di nota».








L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.