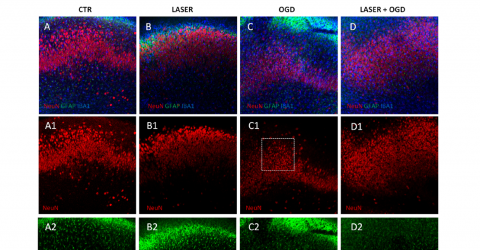
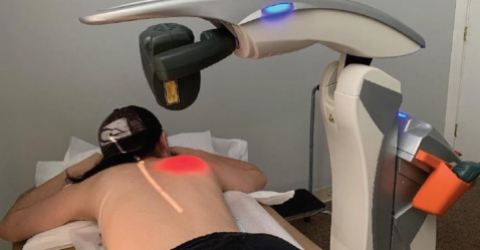




NEUROLASER es el nombre del reciente estudio piloto realizado por un equipo de investigadores de la facultad de medicina de la Hasselt University en colaboración con los médicos de los departamentos de Oncología y Neurología del Jessa Hospital (Hasselt, Bélgica).
El ensayo clínico investigó la eficacia y la seguridad de la terapia de fotobiomodulación (PBMT) erogada mediante fuente láser (M6) en la prevención de la neuropatía periférica inducida por la quimioterapia (CIPN) en pacientes con tumor en el seno.
El equipo dirigido por la Dra. Robijns incluyó a 32 pacientes en el estudio, de los cuales 16 fueron sometidos a PBMT y 16 a tratamiento placebo.
Los datos recogidos mostraron resultados prometedores en términos de prevención. Síntomas como el entumecimiento de las manos y los pies empeoraron significativamente en el grupo de control, mientras que se mantuvieron constantes en el grupo tratado con PMB. La calidad de vida de los pacientes tratados también mejoró en comparación con los pacientes del grupo de control. Todos los tratamientos de con laserterapia han demostrado ser seguros y libres de efectos indeseables.
Para confirmar la aplicabilidad y la eficacia de la terapia láser en la prevención de las neuropatías periféricas inducidas por quimioterapia se necesitan más estudios para aumentar el número de casos. Sin embargo, este estudio preliminar proporciona resultados alentadores sobre la posibilidad de aplicar el sistema M6 en las terapias de apoyo a los pacientes oncológicos, como ya lo demuestran las experiencias anteriores con el tratamiento de la radiodermitis.

“The use of photobiomodulation therapy for the prevention of chemotherapy-induced peripheral neuropathy: a randomized, placebo-controlled pilot trial (NEUROLASER trial)”
Supportive Care Cancer, Mar 21;1-9, 2022






L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.